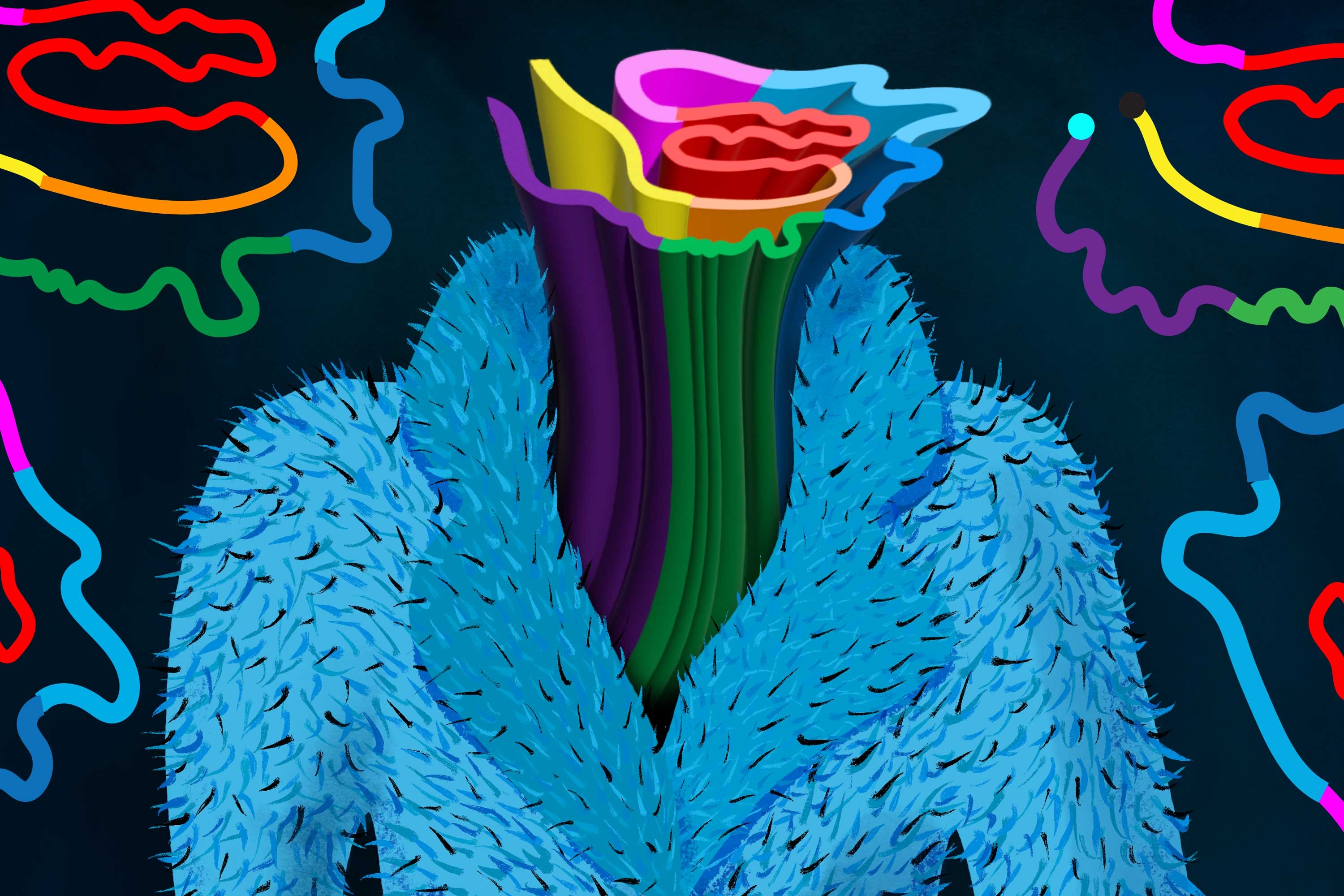
Alzheimer hastalığının en belirgin özelliklerinden biri, Tau adı verilen proteinlerin bir araya gelerek beyinde birbirine dolanmış lifler oluşturmasıdır. Kümelenme ne kadar şiddetliyse, hastalık da o kadar ilerlemiş demektir.
Birçok başka nörodejeneratif hastalıkla da ilişkilendirilen Tau proteini, normal halinde yapısal olarak düzensizdir; ancak patolojik durumda, etrafı gevşek segmentlerle çevrili, iyi düzenlenmiş sert bir çekirdekten oluşur. Bu düzensiz segmentler, Tau'nun diğer moleküllerle nasıl etkileşime gireceğini belirlemeye yardımcı olan bir "bulanık kaplama" oluşturur.
MIT kimyagerleri, ilk kez nükleer manyetik rezonans (NMR) spektroskopisi kullanarak bu tüylü tabakanın yapısını çözebileceklerini gösterdiler. Bulgularının, beyindeki Tau birikimini engelleyen ilaçların geliştirilmesine yardımcı olacağını umuyorlar.
MIT kimya profesörü ve yeni çalışmanın kıdemli yazarı Mei Hong, "Bu Tau fibrillerini küçük moleküllü ilaçlarla parçalamak istiyorsanız, bu ilaçların bu tüylü tabakayı geçmesi gerekiyor" diyor. "Bu, gelecekte önemli bir girişim olacaktır."
MIT yüksek lisans öğrencisi Jia Yi Zhang, bugün Journal of the American Chemical Society dergisinde yayımlanan makalenin baş yazarıdır. Eski MIT doktora sonrası araştırmacısı Aurelio Dregni de makalenin yazarları arasındadır.
Tüylü kürkü analiz etmek
Sağlıklı bir beyinde, Tau proteinleri hücrelere yapılarını veren mikrotübülleri stabilize etmeye yardımcı olur. Bununla birlikte, Tau proteinleri yanlış katlandığında veya başka şekilde değişime uğradığında, Alzheimer ve frontotemporal demans gibi nörodejeneratif hastalıklara katkıda bulunan kümeler oluştururlar.
Tau yumaklarının yapısını belirlemek zor olmuştur çünkü proteinin büyük bir kısmı (yaklaşık yüzde 80'i) oldukça düzensiz olma eğiliminde olan tüylü kılıfta bulunur.
Bu tüylü kaplama, beta tabakaları olarak bilinen katlanmış protein zincirlerinden oluşan sert bir iç çekirdeği çevreler. Hong ve meslektaşları daha önce, moleküller içindeki atom çekirdeklerinin manyetik özelliklerini ölçerek moleküllerin yapılarını ortaya çıkarabilen NMR kullanarak belirli bir Tau fibrilindeki çekirdeğin yapısını analiz etmişlerdir.
Şimdiye kadar çoğu araştırmacı Tau'nun tüylü kaplamasını göz ardı etmiş ve fibrillerin sert çekirdeğine odaklanmıştı; çünkü bu düzensiz segmentler yapılarını o kadar sık değiştiriyor ki, kriyoelektron mikroskopi ve X-ışını kristalografisi gibi standart yapı karakterizasyon teknikleri bunları yakalayamıyor.
Ancak yeni çalışmada araştırmacılar, Tau proteininin tamamını incelemelerine olanak tanıyan NMR teknikleri geliştirdiler. Bir deneyde, en sert amino asitler içindeki protonları mıknatıslayabildiler ve ardından mıknatıslanmanın hareketli amino asitlere aktarılmasının ne kadar sürdüğünü ölçtüler. Bu, mıknatıslanmanın sert bölgelerden esnek bölgelere ve tersine doğru hareketini izlemelerine olanak sağladı.
Bu yaklaşımı kullanarak araştırmacılar, sert ve hareketli segmentler arasındaki yakınlığı tahmin edebildiler. Bu deneyi, tüylü kaplamadaki amino asitlerin farklı hareket derecelerini ölçerek tamamladılar.
Hong, "Artık tam uzunluktaki bir Tau fibrilinin bulanık dış katmanını incelemek için NMR tabanlı bir teknoloji geliştirdik; bu sayede hem dinamik bölgeleri hem de sert çekirdeği yakalayabiliyoruz," diyor.
Protein dinamikleri
Araştırmacılar, bu özel fibril için, yaklaşık 10 farklı alan içeren Tau proteininin genel yapısının, sert çekirdeğin etrafına sarılmış birkaç katmanlı tüylü bir örtüyle, bir tür burritoya benzediğini gösterdi.
Araştırmacılar, protein dinamiklerine ilişkin ölçümlerine dayanarak, bu segmentlerin üç kategoriye ayrıldığını buldular. Fibrilin sert çekirdeği, orta derecede hareketliliğe sahip protein bölgeleriyle çevriliydi, en dinamik segmentler ise en dış katmanda bulunuyordu.
Tüylü örtünün en dinamik bölümleri prolin amino asidi bakımından zengindir. Protein diziliminde, bu prolinler sert çekirdeği oluşturan amino asitlere yakındır ve daha önce kısmen hareketsiz oldukları düşünülüyordu. Bunun yerine, oldukça hareketlidirler; bu da pozitif yüklü prolin bakımından zengin bu bölgelerin, sert çekirdeği oluşturan amino asitlerin pozitif yükleri tarafından itildiğini göstermektedir.
Hong'a göre bu yapısal model, Tau proteinlerinin beyinde nasıl yumak oluşturduğuna dair bir fikir veriyor. Prionların beyindeki sağlıklı proteinlerin yanlış katlanmasına neden olmasına benzer şekilde, yanlış katlanmış Tau proteinlerinin normal Tau proteinlerine yapıştığı ve anormal yapıyı benimsemelerini sağlayan bir şablon görevi gördüğü düşünülüyor.
Prensip olarak, bu normal Tau proteinleri mevcut kısa filamentlerin uçlarına eklenebilir veya yanlarına yığılabilir. Tüylü kaplamanın sert çekirdeği sarması, normal Tau proteinlerinin daha uzun fibriller oluşturmak için filamentlerin uçlarına eklenme olasılığının daha yüksek olduğunu göstermektedir.
Araştırmacılar şimdi, Alzheimer hastalarından alınan yanlış katlanmış Tau proteinlerini şablon olarak kullanarak, normal Tau proteinlerinin Alzheimer hastalığında görülen türde fibrillere dönüşmesini sağlayıp sağlayamayacaklarını araştırmayı planlıyorlar.
Araştırma, Ulusal Sağlık Enstitüleri tarafından finanse edildi.